-Este modelo explicaba por qué las sustancias se combinaban químicamente entre sí sólo en ciertas proporciones.
-El modelo aclaraba que aún existiendo una gran variedad de sustancias diferentes, estas podrían ser explicadas en términos de una cantidad pequeña de constituyentes elementales o elementos.
-En conclusión, este modelo explicaba la mayor parte de la química orgánica del siglo XIX, reduciendo una serie de hechos complejos a una teoría combinatoria realmente simple.
·Modelo atómico de Thomson (1897)
-Es una teoría sobre la estructura atómica propuesta en 1904 por Joseph John Thomson, descubridor del electrón en 1897. El átomo esta compuesto por electrones de carga negativa en un átomo positivo. En 1906, Thomson recibió el premio Nobel de Física por sus investigaciones en la conducción eléctrica en gases.
·Modelo atómico de Rutherford (1911)
-Rutherford trató de ver como era la dispersión de partículas alfa por parte de los átomos de una lámina de oro muy delgada. Rutherford trató de apreciar que esta fracción de partículas rebotadas en dirección opuesta podía ser explicada si se asumía que existían fuertes concentraciones de cargas positivas en el átomo.
-Modelo atómico de Bohr (1913)
-Es un modelo cuantizado del átomo propuesto en 1913 por el físico danés Niels Bohr, para explicar cómo los electrones pueden tener órbitas estables alrededor del núcleo.
-Modelo atómico de Sommerfeld (1916):
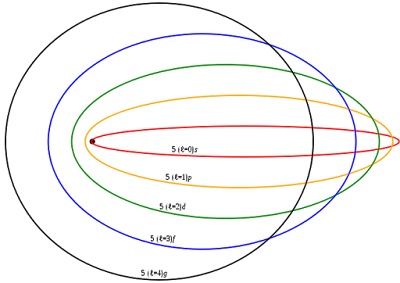
-En 1916, Sommerfeld perfeccionó el modelo atómico de Bohr intentando paliar los dos principales defectos de éste. Esto dio lugar a un nuevo número cuántico: El número cuántico azimutal. Se representa con la letra / y toma valores que van desde 0 hasta n-1. Las órbitas con:
- / = 0 se denominarían posteriormente orbitales o sharp.
- / = 1 se denominarían 2 p o principal.
- / = 2 se denominarían d o diffuse
- / = 3 se denominarían f o fundamental.
-Modelo atómico de Schrödinger (1926):
Es un modelo cuántico no relativista. Se basa en la solución de la ecuación de Schrödinger. para un potencial electrostático con simetría esférica. llamado tambíen átomo hidrogenoide.






No hay comentarios:
Publicar un comentario